Chłoniak Hodgkina coraz skuteczniej kontrolowany

Opublikowano 1 czerwca 2016 23:24
Pozytywna opinia CHNP i zalecenie rejestracji leku to ważna wiadomość dla chorych na chłoniaka Hodgkina z ekspresją CD30 ze zwiększonym ryzykiem nawrotu lub progresji po autologicznym przeszczepie komórek macierzystych szpiku (ang. autologous stem cell transplantation, ASCT).
U około połowy chorych na chłoniaka Hodgkina dochodzi do nawrotu po ASCT, a w przypadku pacjentów obarczonych dodatkowymi czynnikami ryzyka ryzyko nawrotu może być jeszcze wyższe. Koniugat przeciwciała i leku, jakim jest brentuksymab vedotin, byłby pierwszym farmaceutykiem dopuszczonym do obrotu w Europie w tym wskazaniu, w którym aktualnie brak innej opcji terapeutycznej.
Opinia CHNP oparta jest na wynikach badania fazy 3 o akronimie AETHERA. Aktualnie trwa wszechstronna ocena brentuksymabu vedotin w ponad 45 badaniach klinicznych, między innymi w badaniu fazy 3 (ALCANZA) dotyczącym skórnego chłoniaka z komórek T (ang. cutaneous T cell lymphoma, CTCL) z ekspresją CD30 oraz w dwóch dodatkowych badaniach fazy 3, jednym dotyczącym leczenia pierwszego rzutu klasycznego chłoniaka Hodgkina (badanie ECHELON-1) i jednym dotyczącym leczenia pierwszego rzutu chłoniaków z dojrzałych limfocytów T z ekspresją CD30 (badanie ECHELON-2) oraz w badaniach dotyczących wielu innych rodzajów nowotworów złośliwych z ekspresją CD30.
Termin „chłoniak” jest określeniem grupy nowotworów złośliwych wywodzących się z układu limfatycznego. Istnieją dwa główne rodzaje chłoniaków: chłoniaki ziarnicze (chłoniak Hodgkina, czyli ziarnica złośliwa) i chłoniaki nieziarnicze (non-Hodgkin).
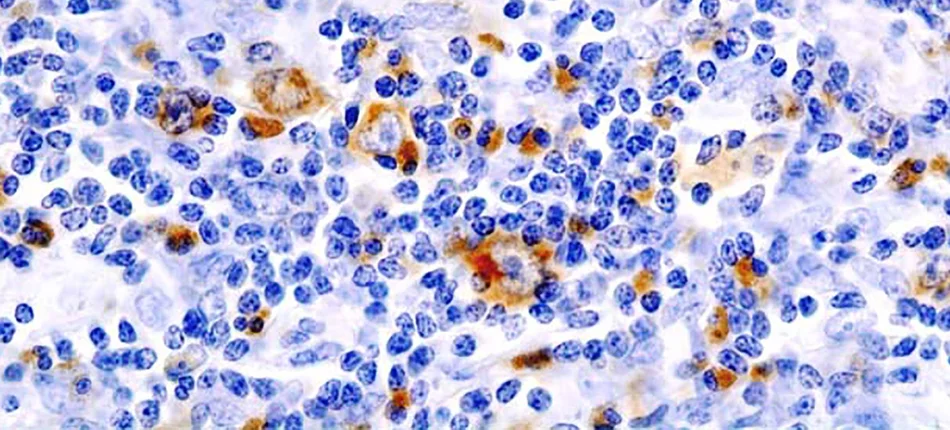
Chłoniak Hodgkina różni się od innych rodzajów chłoniaków obecnością jednego charakterystycznego rodzaju komórek, nazywanych komórkami Reed-Sternberga (na zdjęciu powyżej). Komórki Reed-Sternberga wykazują ekspresję CD30.
Źródło: materiały prasowe