Thinkstock / Getty Images[/caption]
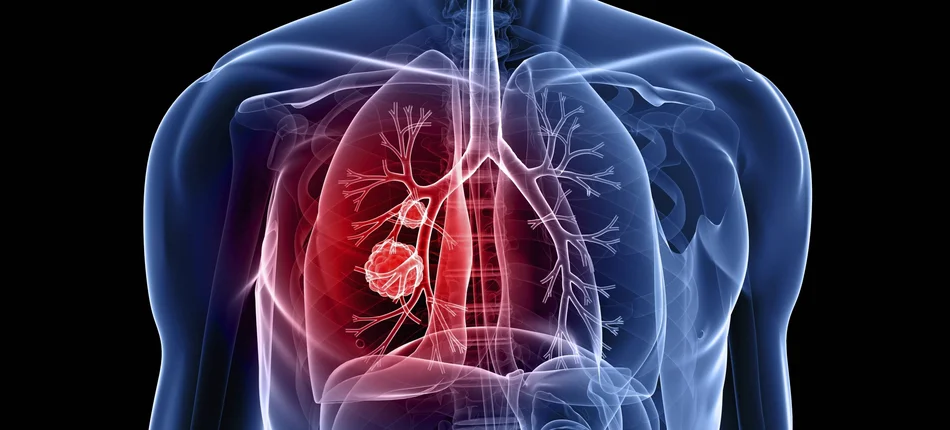
Thinkstock / Getty Images[/caption]Amerykańska Agencja Żywości i Leków (FDA) zarejestrowała niwolumab – inhibitor PD-1, do stosowania u wcześniej leczonych pacjentów z zaawansowanym płaskonabłonkowym niedrobnokomórkowym rakiem płuca (NDRP). To pierwszy lek immunnoonkologiczny zarejestrowany w tym wskazaniu.
Rak płuca, wg danych Światowej Organizacji Zdrowia, jest każdego roku powodem 1,5 mln zgonów. Jest też główną przyczyną śmierci z powodu chorób nowotworowych. Niedrobnokomórkowy rak płuca stanowi około 85 proc. wszystkich przypadków nowotworu płuca. Globalny wskaźnik przeżycia pięcioletniego w NDRP w I stadium zaawansowania wynosi od 47 do 50 proc. , a w przypadku NDRP w IV stadium zaawansowania wskaźnik przeżycia pięcioletniego spada do 2 proc.
FDA podjęła decyzję o rejestracji niwolumabu we wskazaniu NDPR na podstawie wyników badania fazy 3 CheckMate–017, oceniającego skuteczność stosowania niwolumabu w porównaniu z docetakselem u wcześniej leczonych pacjentów z zaawansowanym lub przerzutowym płaskonabłonkowym NDRP. W badaniu zrandomizowano 272 pacjentów do grupy otrzymującej niwolumab lub do grupy otrzymującej docetaksel. Badanie to zostało zakończone przed terminem. Ocena przeprowadzona przez niezależną Komisję ds. Monitorowania Danych (DMC) wykazała, bowiem że badanie osiągnęło swój punkt końcowy, powodując dłuższe przeżycia całkowite u pacjentów otrzymujących niwolumab w porównaniu z grupą kontrolną.
Wcześniej niwolumab został już zarejestrowany przez FDA do stosowania u pacjentów z nieoperacyjnym lub przerzutowym czerniakiem.
Źródło: materiały prasowe